В зависимости от степени диссоциации различают электролиты сильные и слабые. К - константа диссоциации, которая зависит от температуры и природы электролита и растворителя, но не зависит от концентрации электролита. Реакции между ионами в растворах электролитов идут практически до конца в сторону образования осадков, газов и слабых электролитов.
Электроли́т - вещество, которое проводит электрический ток вследствие диссоциации на ионы, что происходит в растворах и расплавах, или движения ионов в кристаллических решётках твёрдых электролитов. Примерами электролитов могут служить водные растворы кислот, солей и оснований и некоторые кристаллы (например, иодид серебра, диоксид циркония).
Как определить сильные и слабые электролиты
Одновременно в электролите протекают процессы ассоциации ионов в молекулы. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике). Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например электролит золочения).

Основным объектом исследования и разработки в гальванотехнике являются электролиты для обработки поверхности и нанесения на неё покрытий. При химическом травлении металлов названия электролитов определяется названием основных кислот или щелочей, способствующих растворению металла. Так формируется групповое название электролитов. Иногда разница (особенно в величине поляризуемости) между электролитами разных групп нивелируется добавками, содержащимися в электролитах.
Электролиты и электролитическая диссоциация
Поэтому такое название не может являться классификационным (то есть групповым), а должно служить дополнительным подгрупповым наименованием электролита. Если плотность электролита во всех ячейках аккумулятора нормальная или близка к норме (1,25-1,28 г/см3), а НРЦ не ниже 12,5 В, то необходимо проверить на обрыв цепи внутри аккумулятора. При низкой плотности электролита во всех ячейках батарею следует зарядить до стабилизации плотности.
В технике[править править вики-текст]
При переходе от одного состояния в другое, показатели напряжения и плотности электролита линейно изменяются в определенных пределах (рис.4 и табл.1). Чем глубже происходит разряд аккумулятора, тем ниже плотность электролита. Соответственно, в объеме электролита содержится количество серной кислоты, необходимое для полного использования в реакции активного вещества пластин.
Ионная проводимость присуща многим химическим соединениям, обладающим ионным строением, например солям в твердом или расплавленном состояниях, а также многим водным и неводным растворам. Под электролитической диссоциацией понимается распад молекул электролита в растворе с образованием положительно и отрицательно заряженных ионов - катионов и анионов. Степень диссоциации часто выражают в процентах. Это объясняется тем, что концентрации металлических меди и серебра введены в константу равновесия.

Объясняется это тем, что концентрация воды во время реакций в водных растворах изменяется очень незначительно. Поэтому принимается, что концентрация остается постоянной и вводится в константу равновесия. Поскольку электролиты в растворах образуют ионы, то для отражения сущности реакций часто используют так называемые ионные уравнения реакций.
Термин электролит широко используется в биологии и медицине. Процесс распада молекул в растворе или расплаве электролита на ионы называется электролитической диссоциацией. Поэтому в электролитах диссоциирована определённая доля молекул вещества. Между этими двумя группами чёткой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом - слабого.
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3. Сильные и слабые электролиты
Материал этого раздела частично вам знаком по ранее изученным школьным курсам химии и из предыдущего раздела. Кратко повторим, что вам известно, и познакомимся с новым материалом.
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Имеется ряд простых, но несомненных
доказательств того, что некоторые вещества в
водных растворах распадаются на частицы. Так,
водные растворы серной H 2 SO 4 , азотной HNO 3 ,
хлорной HClO 4 , хлороводородной (соляной) HCl,
уксусной CH 3 COOH и других кислот имеют кислый
вкус. В формулах кислот общей частицей является
атом водорода, и можно предположить, что он (в
виде иона) является причиной одинакового вкуса
всех этих столь различных веществ.
Образующиеся при диссоциации в водном растворе
ионы водорода придают раствору кислый вкус,
поэтому такие вещества и названы кислотами. В
природе только ионы водорода имеют кислый вкус.
Они создают в водном растворе так называемую
кислотную (кислую) среду.
Запомните, когда вы говорите «хлороводород», то имеете в виду газообразное и кристаллическое состояние этого вещества, но для водного раствора следует говорить «раствор хлороводорода», «хлороводородная кислота» или использовать общепринятое название «соляная кислота», хотя состав вещества в любом состоянии выражается одной и той же формулой – НСl.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений.
Хлороводородная HCl, бромоводородная HBr и
йодоводородная HI кислоты реагируют с цинком
одинаково, несмотря на свой различный состав, т.
к. в действительности с цинком реагирует не
кислота:
Zn + 2НСl = ZnСl 2 + Н2,
а ионы водорода:
Zn + 2H + = Zn 2+ + Н 2 ,
и образуются газообразный водород и ионы цинка.
Смешивание некоторых растворов солей, например
хлорида калия KCl и нитрата натрия NaNO 3 , не
сопровождается заметным тепловым эффектом, хотя
после выпаривания раствора образуется смесь
кристаллов четырех веществ: исходных – хлорида
калия и нитрата натрия – и новых – нитрата калия
КNO 3 и хлорида натрия NaCl. Можно предположить,
что в растворе две исходные соли полностью
распадаются на ионы, которые при его выпаривании
образуют четыре кристаллических вещества:
Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы.
Изучение продуктов электролиза позволяет
приписать ионам положительные или отрицательные
заряды. Очевидно, если кислота, например азотная
НNO 3 , диссоциирует, предположим, на два иона
и при электролизе водного раствора на катоде
(отрицательно заряженный электрод) выделяется
водород, то, следовательно, в растворе имеются
положительно заряженные ионы водорода Н + .
Тогда уравнение диссоциации следует записать
так:
НNO 3 = Н + + .
Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя).
Электролиты
– кислоты, основания или
соли, водные растворы которых проводят
электрический ток в результате диссоциации.
Вещества, не диссоциирующие в водном растворе на
ионы и растворы которых не проводят
электрический ток, называются неэлектролитами
.
Диссоциация электролитов количественно
характеризуется степенью диссоциации
– отношением числа распавшихся на ионы
«молекул» (формульных единиц) к общему числу
«молекул» растворенного вещества. Степень
диссоциации обозначается греческой буквой . Например, если из
каждых 100 «молекул» растворенного вещества 80
распадаются на ионы, то степень диссоциации
растворенного вещества равна: = 80/100 = 0,8, или 80%.
По способности к диссоциации (или, как говорят,
«по силе») электролиты разделяют на сильные
,
средние
и слабые
. По степени
диссоциации к сильным электролитам относят те из
них, для растворов которых > 30%, к слабым – < 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
В случае водных растворов
к сильным электролитам
( > 30%) относят
перечисленные ниже группы соединений.
1
. Многие неорганические кислоты,
например хлороводородная НCl, азотная HNO 3 ,
серная H 2 SО 4 в разбавленных растворах.
Самая сильная неорганическая кислота – хлорная
НСlО 4 .
Сила некислородных кислот возрастает в ряду
однотипных соединений при переходе вниз по
подгруппе кислотообразующих элементов:
HCl – HBr – HI.
Фтороводородная (плавиковая) кислота HF растворяет стекло, но это вовсе не говорит о ее силе. Эта кислота из бескислородных галогенсодержащих относится к кислотам средней силы из-за высокой энергии связи Н–F, способности молекул HF к объединению (ассоциации) благодаря сильным водородным связям, взаимодействия ионов F – с молекулами НF (водородные связи) с образованием ионов и других более сложных частиц. В результате концентрация ионов водорода в водном растворе этой кислоты оказывается значительно пониженной, поэтому фтороводородную кислоту считают средней силы.
Фтороводород реагирует с диоксидом кремния, входящим в состав стекла, по уравнению:SiO 2 + 4HF = SiF 4 + 2H 2 O.
Фтороводородную кислоту нельзя хранить в стеклянных сосудах. Для этого используют сосуды из свинца, некоторых пластмасс и стекла, стенки которых покрыты изнутри толстым слоем парафина. Если для «травления» стекла использовать газообразный фтороводород, то поверхность стекла становится матовой, что используется для нанесения на стекло надписей и различных рисунков. «Травление» стекла водным раствором фтороводородной кислоты приводит к разъеданию поверхности стекла, которая остается прозрачной. В продаже обычно бывает 40%-й раствор плавиковой кислоты.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
Если элемент образует несколько кислородных
кислот, то наибольшей силой обладает кислота, в
которой кислотообразующий элемент имеет самую
высокую валентность. Так, в ряду кислот НСlО
(хлорноватистая) – НСlО 2 (хлористая) – НСlО 3
(хлорноватая) – НСlО 4 (хлорная) последняя
наиболее сильная.
Один объем воды растворяет около двух объемов хлора. Хлор (примерно половина его) взаимодействует с водой:
Cl 2 + H 2 O = HCl + HСlO.
Хлороводородная кислота является сильной, в ее водном растворе практически нет молекул HCl. Правильнее уравнение реакции записать так:
Cl 2 + H 2 O = H + + Cl – + HClO – 25 кДж/моль.
Образующийся раствор называют хлорной водой.
Хлорноватистая кислота – быстродействующий окислитель, поэтому ее применяют для отбеливания тканей.
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Щелочами называют растворимые в воде основания. К ним относят также гидроксиды элементов главной подгруппы II группы (щелочно-земельные металлы) и гидроксид аммония (водный раствор аммиака). Иногда щелочами считают те гидроксиды, которые в водном растворе создают высокую концентрацию гидроксид-ионов. В устаревшей литературе вы можете встретить в числе щелочей карбонаты калия К 2 СО 3 (поташ) и натрия Na 2 CO 3 (сода), гидрокарбонат натрия NaHCO 3 (питьевая сода), буру Na 2 B 4 O 7 , гидросульфиды натрия NaHS и калия KHS и др.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень:
Са(ОН) 2 = Са 2+ + 2ОН – .
3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа:
FeCl 3 = Fe 3+ + 3Cl – .
В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения.
1 . Вода H 2 O – важнейший электролит.
2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Заметим, что угольная кислота в формуле H 2 CO 3
не существует. При растворении углекислого газа
СО 2 в воде образуется его гидрат СО 2 Н 2 О,
который мы для удобства расчетов записываем
формулой H 2 CO 3 , и уравнение реакции
диссоциации выглядит так:
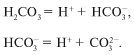
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
Точно так же ступенчато диссоциируют и другие
многоосновные кислоты: Н 3 РО 4
(фосфорная), H 2 SiO 3 (кремниевая), H 3 BO 3
(борная). В водном растворе диссоциация
практически проходит лишь по первой ступени. Как
осуществить диссоциацию по последней ступени?
3
. Гидроксиды многих элементов, например
Аl(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Fe(OH) 3 и др.
Все эти гидроксиды диссоциируют в водном
растворе ступенчато, например гидроксид железа
Fe(OH) 3:

В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
Осно"вные свойства гидроксидов одного и того же
элемента усиливаются с уменьшением валентности
элемента. Так, осно"вные свойства дигидроксида
железа Fe(OH) 2 выражены сильнее, чем у
тригидроксида Fe(OH) 3 . Это утверждение
равносильно тому, что кислотные свойства Fe(OH) 3
проявляются сильнее, чем у Fe(OH) 2 .
4
. Гидроксид аммония NH 4 OH.
При растворении газообразного аммиака NH 3 в
воде получается раствор, который очень слабо
проводит электрический ток и имеет
горько-мыльный вкус. Среда раствора осно"вная,
или щелочная. Объясняется такое поведение
аммиака следующим образом. При растворении
аммиака в воде образуется гидрат аммиака NH 3 Н 2 О,
которому условно мы приписываем формулу
несуществующего гидроксида аммония NH 4 OH,
считая, что это соединение диссоциирует с
образованием иона аммония и гидроксид-иона ОН – :
NH 4 OH = + ОН – .
5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато.
К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень.
ЭЛЕКТРОЛИТЫ – вещества, растворы или расплавы которых проводят электрический ток.
НЕЭЛЕКТРОЛИТЫ – вещества, растворы или расплавы которых не проводят электрический ток.
Диссоциация – распад соединений на ионы.
Степень диссоциации – отношение числа продиссоциированных на ионы молекул к общему числу молекул в растворе.
СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ при растворении в воде практически полностью диссоциируют на ионы.
При написании уравнений диссоциации сильных электролитов ставят знак равенства.
К сильным электролитам относятся:
· Растворимые соли (смотри таблицу растворимости );
· Многие неорганические кислоты: HNO 3 , H 2 SO 4 ,HClO 3 , HClO 4 , HMnO 4 , HCl, HBr, HI (смотри кислоты-сильные электролиты в таблице растворимости );
· Основания щелочных (LiOH, NaOH,KOH) и щелочноземельных (Ca(OH) 2 , Sr(OH) 2 , Ba(OH) 2) металлов (смотри основания-сильные электролиты в таблице растворимости ).
СЛАБЫЕ ЭЛЕКТРОЛИТЫ в водных растворах лишь частично (обратимо) диссоциируют на ионы.
При написании уравнений диссоциации слабых электролитов ставят знак обратимости.
К слабым электролитам относятся:
· Почти все органические кислоты и вода (Н 2 О);
· Некоторые неорганические кислоты: H 2 S, H 3 PO 4 ,HClO 4 , H 2 CO 3 , HNO 2 , H 2 SiO 3 (смотри кислоты-слабые электролиты в таблице растворимости );
· Нерастворимые гидроксиды металлов (Mg(OH) 2 ,Fe(OH) 2 , Zn(OH) 2) (смотри основания- c лабые электролиты в таблице растворимости ).
На степень электролитической диссоциации влияет ряд факторов:
природа растворителя и электролита : сильными электролитами являются вещества с ионными и ковалентными сильно-полярными связями; хорошей ионизирующей способностью, т.е. способностью вызывать диссоциацию веществ, обладают растворители с большой диэлектрической проницаемостью, молекулы которых полярны (например, вода);
температура : поскольку диссоциация - процесс эндотермический, повышение температуры повышает значение α;
концентрация : при разбавлении раствора степень диссоциации возрастает, а с увеличением концентрации - уменьшается;
стадия процесса диссоциации : каждая последующая стадия менее эффективна, чем предыдущая, примерно в 1000–10 000 раз; например, для фосфорной кислоты α 1 > α 2 > α 3:
H3PО4⇄Н++H2PО−4 (первая стадия, α 1),
H2PО−4⇄Н++HPО2−4 (вторая стадия, α 2),
НPО2−4⇄Н++PО3−4 (третья стадия, α 3).
По этой причине в растворе данной кислоты концентрация ионов водорода наибольшая, а фосфат-ионов РО3−4 - наименьшая.
1. Растворимость и степень диссоциации вещества между собой не связаны. Например, слабым электролитом является хорошо (неограниченно) растворимая в воде уксусная кислота.
2. В растворе слабого электролита меньше других содержится тех ионов, которые образуются на последней стадии электролитической диссоциации
На степень электролитической диссоциации влияет также добавление других электролитов : например, степень диссоциации муравьиной кислоты
HCOOH ⇄ HCOO − + H +
уменьшается, если в раствор внести немного формиата натрия. Эта соль диссоциирует с образованием формиат-ионов HCOO − :
HCOONa → HCOO − + Na +
В результате в растворе концентрация ионов НСОО– повышается, а согласно принципу Ле Шателье, повышение концентрации формиат-ионов смещает равновесие процесса диссоциации муравьиной кислоты влево, т.е. степень диссоциации уменьшается.
Закон разбавления Оствальда - соотношение, выражающее зависимость эквивалентной электропроводностиразбавленного раствора бинарного слабого электролита от концентрации раствора:
Здесь - константа диссоциации электролита, - концентрация, и - значения эквивалентной электропроводности при концентрации и при бесконечном разбавлении соответственно. Соотношение является следствием закона действующих масс и равенства
где - степень диссоциации.
Закон разбавления Оствальда выведен В.Оствальдом в 1888 году и им же подтвержден опытным путём. Экспериментальное установление правильности закона разбавления Оствальда имело большое значение для обоснования теории электролитической диссоциации.
Электролитическая диссоциация воды. Водородный показатель рН Вода представляет собой слабый амфотерный электролит: Н2О Н+ + ОН- или, более точно: 2Н2О= Н3О+ + ОН- Константа диссоциации воды при 25оС равна: Такое значение константы соответствует диссоциации одной из ста миллионов молекул воды, поэтому концентрацию воды можно считать постоянной и равной 55,55 моль/л (плотность воды 1000 г/л, масса 1 л 1000 г, количество вещества воды 1000г:18г/моль=55,55 моль, С=55,55 моль: 1 л =55,55 моль/л). Тогда Эта величина постоянная при данной температуре (25оС), она называется ионным произведением воды KW: Диссоциация воды – процесс эндотермический, поэтому с повышением температуры в соответствии с принципом Ле-Шателье диссоциация усиливается, ионное произведение возрастает и достигает при 100оС значения 10-13. В чистой воде при 25оС концентрации ионов водорода и гидроксила равны между собой: = = 10-7 моль/л Растворы, в которых концентрации ионов водорода и гидроксила равны между собой, называются нейтральными. Если к чистой воде прибавить кислоту, концентрация ионов водорда повысится и станет больше, чем 10-7 моль/л, среда станет кислой, при этом концентрация ионов гидроксила мгновенно изменится так, чтобы ионное произведение воды сохранило свое значение 10-14. Тоже самое будет происходить и при добавлении к чистой воде щелочи. Концентрации ионов водорода и гидроксила связаны между собой через ионное произведение, поэтому, зная концентрацию одного из ионов, легко вычислить концентрацию другого. Например, если = 10-3 моль/л, то = KW/ = 10-14/10-3 = 10-11 моль/л, или, если = 10-2 моль/л, то = KW/ = 10-14/10-2 = 10-12 моль/л. Таким образом, концентрация ионов водорода или гидроксила может служить количественной характеристикой кислотности или щелочности среды. На практике пользуются не концентрациями ионов водорода или гидроксила, а водородным рН или гидроксильным рОН показателями. Водородный показатель рН равен отрицательному десятичному логарифму концентрации ионов водорода: рН = - lg Гидроксильный показатель рОН равен отрицательному десятичному логарифму концентрации ионов гидроксила: рОН = - lg Легко показать, прологарифмировав ионное произведение воды, что рН + рОН = 14 Если рН среды равен 7 - среда нейтральная, если меньше 7 - кислая, причем чем меньше рН, тем выше концентрация ионов водорода. pН больше 7 – среда щелочная, чем больше рН, тем выше концентрация ионов гидроксила.
Соли, их свойства, гидролиз
Ученица 8 класс Б школы № 182
Петрова Полина
Учитель химии:
Харина Екатерина Алексеевна
МОСКВА 2009
В быту мы привыкли иметь дело лишь с одной солью – поваренной, т.е. хлоридом натрия NaCl. Однако в химии солями называют целый класс соединений. Соли можно рассматривать как продукты замещения водорода в кислоте на металл. Поваренную соль, например, можно получить из соляной кислоты по реакции замещения:
2Na + 2HCl = 2NaCl + H 2 .
кислота соль
Если вместо натрия взять алюминий, образуется другая соль – хлорид алюминия:
2Al + 6HCl = 2AlCl 3 + 3H 2
Соли – это сложные вещества, состоящие из атомов металлов и кислотных остатков. Они являются продуктами полного или частичного замещения водорода в кислоте на металл или гидроксильной группы в основании на кислотный остаток. Например, если в серной кислоте H 2 SO 4 заместить на калий один атом водорода, получим соль KHSO 4 , а если два – K 2 SO 4 .
Различают несколько типов солей.
| Типы солей | Определение | Примеры солей |
| Средние | Продукт полного замещения водорода кислоты на металл. Ни атомов Н, ни ОН-групп не содержат. | Na 2 SO 4 сульфат натрия CuCl 2 хлорид меди (II) Ca 3 (PO 4) 2 фосфат кальция Na 2 CO 3 карбонат натрия (кальцинированная сода) |
| Кислые | Продукт неполного замещения водорода кислоты на металл. Содержат в своем составе атомы водорода. (Они образованны только многоосновными кислотами) | CaHPO 4 гидрофосфат кальция Ca(H 2 PO 4) 2 дигидрофосфат кальция NaHCO 3 гидрокарбонат натрия (питьевая сода) |
| Основные | Продукт неполного замещения гидроксогрупп основания на кислотный остаток. Включают ОН-группы. (Образованны только многокислотными основаниями) | Cu(OH)Cl гидроксохлорид меди (II) Ca 5 (PO 4) 3 (OH) гидроксофосфат кальция (CuOH) 2 CO 3 гидроксокарбонат меди (II) (малахит) |
| Смешанные | Соли двух кислот | Ca(OCl)Cl – хлорная известь |
| Двойные | Соли двух металлов | K 2 NaPO 4 – ортофосфат дикалия-натрия |
| Кристаллогидраты | Содержат кристаллизационную воду. При нагревании они обезвоживаются – теряют воду, превращаясь в безводную соль. | CuSO 4 . 5H 2 O – пятиводный сульфат меди(II) (медный купорос) Na 2 CO 3 . 10H 2 O – десятиводный карбонат натрия (сода) |
Способы получения солей.
1. Соли можно получить, действуя кислотами на металлы, основные оксиды и основания:
Zn + 2HCl ZnCl 2 + H 2
хлорид цинка
3H 2 SO 4 + Fe 2 O 3 Fe 2 (SO 4) 3 + 3H 2 O
сульфат железа (III)
3HNO 3 + Cr(OH) 3 Cr(NO 3) 3 + 3H 2 O
нитрат хрома (III)
2. Соли образуются при реакции кислотных оксидов со щелочами, а также кислотных оксидов с основными оксидами:
N 2 O 5 + Ca(OH) 2 Ca(NO 3) 2 + H 2 O
нитрат кальция
SiO 2 + CaO CaSiO 3
силикат кальция
3. Соли можно получить при взаимодействии солей с кислотами, щелочами, металлами, нелетучими кислотными оксидами и другими солями. Такие реакции протекают при условии выделения газа, выпадения осадка, выделения оксида более слабой кислоты или выделения летучего оксида.
Ca 3 (PO4) 2 + 3H 2 SO 4 3CaSO 4 + 2H 3 PO 4
ортофосфат кальция сульфат кальция
Fe 2 (SO 4) 3 + 6NaOH 2Fe(OH) 3 + 3Na 2 SO 4
сульфат железа (III) сульфат натрия
CuSO 4 + Fe FeSO 4 + Cu
сульфат меди (II) сульфат железа (II)
CaCO 3 + SiO 2 CaSiO 3 + CO 2
карбонат кальция силикат кальция
Al 2 (SO 4) 3 + 3BaCl 2 3BaSO 4 + 2AlCl 3
сульфат хлорид сульфат хлорид
алюминия бария бария алюминия
4. Соли бескислородных кислот образуются при взаимодействии металлов с неметаллами:
2Fe + 3Cl 2 2FeCl 3
хлорид железа (III)
Физические свойства.
Соли – твердые вещества различного цвета. Растворимость в воде их различна. Растворимы все соли азотной и уксусной кислот, а также соли натрия и калия. О растворимости в воде других солей можно узнать из таблицы растворимости.
Химические свойства.
1) Соли реагируют с металлами.
Так как эти реакции протекают в водных растворах, то для опытов нельзя применять Li, Na, K, Ca, Ba и другие активные металлы, которые при обычных условиях реагируют с водой, либо проводить реакции в расплаве.
CuSO 4 + Zn ZnSO 4 + Cu
Pb(NO 3) 2 + Zn Zn(NO 3) 2 + Pb
2) Соли реагируют с кислотами. Эти реакции протекают, когда более сильная кислота вытесняет более слабую, при этом выделяется газ или выпадает осадок.
При проведении этих реакций обычно берут сухую соль и действуют концентрированной кислотой.
BaCl 2 + H 2 SO 4 BaSO 4 + 2HCl
Na 2 SiO 3 + 2HCl 2NaCl + H 2 SiO 3
3) Соли реагируют со щелочами в водных растворах.
Это способ получения нерастворимых оснований и щелочей.
FeCl 3 (p-p) + 3NaOH(p-p) Fe(OH) 3 + 3NaCl
CuSO 4 (p-p) + 2NaOH (p-p) Na 2 SO 4 + Cu(OH) 2
Na 2 SO 4 + Ba(OH) 2 BaSO 4 + 2NaOH
4) Соли реагируют с солями.
Реакции протекают в растворах и используются для получения практически нерастворимых солей.
AgNO 3 + KBr AgBr + KNO 3
CaCl 2 + Na 2 CO 3 CaCO 3 + 2NaCl
5) Некоторые соли при нагревании разлагаются.
Характерным примером такой реакции является обжиг известняка, основной составной частью которого является карбонат кальция:
CaCO 3 CaO + CO2 карбонат кальция
1. Некоторые соли способны кристаллизироваться с образованием кристаллогидратов.
Сульфат меди (II) CuSO 4 – кристаллическое вещество белого цвета. При его растворении в воде происходит разогревание и образуется раствор голубого цвета. Выделение теплоты и изменение цвета – это признаки химической реакции. При выпаривании раствора выделяется кристаллогидрат CuSO 4 . 5H 2 O (медный купорос) . Образование этого вещества свидетельствует о том, что сульфат меди (II) реагирует с водой:
CuSO 4 + 5H 2 O CuSO 4 . 5H 2 O + Q
белого цвета сине-голубого цвета
Применение солей.
Большинство солей широко используется в промышленности и в быту. Например, хлорид натрия NaCl, или поваренная соль, незаменим в приготовлении пищи. В промышленности хлорид натрия используется для получения гидроксида натрия, соды NaHCO 3 , хлора, натрия. Соли азотной и ортофосфорной кислот в основном являются минеральными удобрениями. Например, нитрат калия KNO 3 – калийная селитра. Она также входит в состав пороха и других пиротехнических смесей. Соли применяются для получения металлов, кислот, в производстве стекла. Многие средства защиты растений от болезней, вредителей, некоторые лекарственные вещества также относятся к классу солей. Перманганат калия KMnO 4 часто называют марганцовкой. В качестве строительного материала используются известняки и гипс – CaSO 4 . 2H 2 O, который также применяется в медицине.
Растворы и растворимость.
Как уже указывалось ранее, растворимость является важным свойством солей. Растворимость - способность вещества образовывать с другим веществом однородную, устойчивую систему переменного состава, состоящую из двух или большего числа компонентов.
Растворы – это однородные системы, состоящие из молекул растворителя и частиц растворенного вещества.
Так, например, раствор поваренной соли состоит из растворителя – воды, растворенного вещества – ионов Na + ,Cl - .
Ионы (от греч. ión - идущий), электрически заряженные частицы, образующиеся при потере или присоединении электронов (или других заряженных частиц) атомами или группами атомов. Понятие и термин «ион» ввёл в 1834 М. Фарадей, который, изучая действие электрического тока на водные растворы кислот, щелочей и солей, предположил, что электропроводность таких растворов обусловлена движением ионов. Положительно заряженные ионы, движущиеся в растворе к отрицательному полюсу (катоду), Фарадей назвал катионами, а отрицательно заряженные, движущиеся к положительному полюсу (аноду), - анионами.
По степени растворимости в воде вещества делятся на три группы:
1) Хорошо растворимые;
2) Малорастворимые;
3) Практически нерастворимые.
Многие соли хорошо растворимы в воде. При решении вопроса о растворимости в воде других солей придется пользоваться таблицей растворимости.
Хорошо известно, что одни вещества в растворенном или расплавленном виде проводят электрический ток, другие в тех же условиях ток не проводят.
Вещества, распадающиеся на ионы в растворах или расплавах и поэтому проводящие электрический ток, называют электролитами .
Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами .
К электролитам относятся кислоты, основания и почти все соли. Сами электролиты электрический ток не проводят. В растворах и расплавах они распадаются на ионы, благодаря чему и протекает ток.
Распад электролитов на ионы при растворении их в воде называется электролитической диссоциацией . Ее содержание сводится к трем следующим положениям:
1) Электролиты при растворении в воде распадаются (диссоциируют) на ионы – положительные и отрицательные.
2) Под действием электрического тока ионы приобретают направленное движение: положительно заряженные ионы движутся к катоду и называются – катионы, а отрицательно заряженные ионы движутся к аноду и называются – анионами.
3) Диссоциация – обратимый процесс: параллельно с распадом молекул на ионы (диссоциацией) протекает процесс соединения ионов (ассоциация).
обратимость
Сильные и слабые электролиты.
Для количественной характеристики способности электролита распадаться на ионы введено понятие степени диссоциации (α), т. Е. Отношения числа молекул, распавшихся на ионы, кобщему числу молекул. Например, α = 1 говорит о том, что электролит полностью распался на ионы, а α = 0,2 означает, что продиссоциировала лишь каждая пятая из его молекул. При разбавлении концентрированного раствора, а также при нагревании его электропроводность повышается, так как возрастает степень диссоциации.
В зависимости от величины α электролиты условно делятся на сильные (диссоциируют практически нацело, (α 0,95) средней силы (0,95
Сильными электролитами являются многие минеральные кислоты (HCl, HBr, HI, H 2 SO 4 , HNO 3 и др.), щелочи (NaOH, KOH, Ca(OH) 2 и др.), почти все соли. К слабым принадлежат растворы некоторых минеральных кислот (H 2 S, H 2 SO 3 , H 2 CO 3 , HCN, HClO), многие органические кислоты (например, уксусная CH 3 COOH), водный раствор аммиака (NH 3 . 2 O), вода, некоторые соли ртути (HgCl 2). К электролитам средней силы часто относят плавиковую HF, ортофосфорную H 3 PO 4 и азотистую HNO 2 кислоты.
Гидролиз солей.
Термин « гидролиз » произошел от греческих слов hidor (вода) и lysis (разложение). Под гидролизом обычно понимают обменную реакцию между веществом и водой. Гидролитические процессы чрезвычайно распространены в окружающей нас природе (как живой, так и неживой), а также широко используются человеком в современных производственных и бытовых технологиях.
Гидролизом соли называется реакция взаимодействия ионов, входящих в состав соли, с водой, которая приводит к образованию слабого электролита и сопровождается изменением среды раствора.
Гидролизу подвергаются три типа солей:
а) соли, образованные слабым основанием и сильной кислотой (CuCl 2 , NH 4 Cl, Fe 2 (SO 4) 3 - протекает гидролиз по катиону)
NH 4 + + H 2 O NH 3 + H 3 O +
NH 4 Cl + H 2 O NH 3 . H 2 O + HCl
Реакция среды – кислая.
б) соли, образованные сильным основанием и слабой кислотой (К 2 CO 3 , Na 2 S - протекает гидролиз по аниону)
SiO 3 2- + 2H 2 O H 2 SiO 3 + 2OH -
K 2 SiO 3 +2H 2 O H 2 SiO 3 +2KOH
Реакция среды – щелочная.
в) соли, образованные слабым основанием и слабой кислотой (NH 4) 2 CO 3 , Fe 2 (CO 3) 3 – протекает гидролиз по катиону и по аниону.
2NH 4 + + CO 3 2- + 2H 2 O 2NH 3 . H 2 O + H 2 CO 3
(NH 4) 2 CO 3 + H 2 O 2NH 3 . H 2 O + H 2 CO 3
Часто реакция среды – нейтральная.
г) соли образованные сильным основанием и сильной кислотой (NaCl, Ba(NO 3) 2) гидролизу не подвержены.
В ряде случаев гидролиз протекает необратимо (как говорят, идет до конца). Так при смешении растворов карбоната натрия и сульфата меди выпадает голубой осадок гидратированной основной соли, которая при нагревании теряет часть кристаллизационной воды и приобретает зеленый цвет – превращается в безводный основный карбонат меди – малахит:
2CuSO 4 + 2Na 2 CO 3 + H 2 O (CuOH) 2 CO 3 + 2Na 2 SO 4 + CO 2
При смешении растворов сульфида натрия и хлорида алюминия гидролиз также идет до конца:
2AlCl 3 + 3Na 2 S + 6H 2 O 2Al(OH) 3 + 3H 2 S + 6NaCl
Поэтому Al 2 S 3 нельзя выделить из водного раствора. Эту соль получают из простых веществ.


